보도자료
-
92
KIST, 세계 최초로 근육세포 융합의 비밀을 풀다
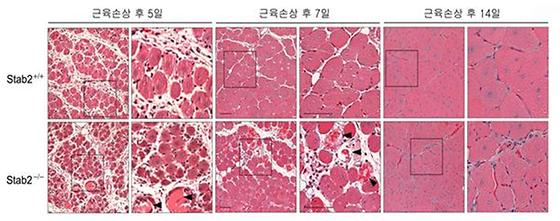
KIST, 세계 최초로 근육세포 융합의 비밀을 풀다 - 정상 근육세포에 작용하는 ‘포스파티딜세린’ 인식 수용체 규명 - 근육세포 융합의 분자적 기전을 밝히는 돌파구 마련 근육은 인체의 활동성에 매우 중요한 근골격계 유지 및 대사과정에 중요한 역할을 하는 기관이다. 근육 조직은 많은 근섬유로 구성되어 있으며, 각각의 근섬유는 근육세포의 융합에 의해 형성된 하나의 다핵세포로 구성된다. 현재까지 근육세포 융합에 작용하는 다양한 분자들이 밝혀지고 많은 모델들이 제시되었다. 하지만 근육세포 융합의 정확한 분자적 기전을 규명하기 위해서는 아직 많은 연구들이 수행되어야하는 상황이다. 한국과학기술연구원(KIST, 원장 이병권) 김인산 박사, 동국의대 박승윤 교수 연구팀은 근육형성 과정에서 근육 세포의 융합과정에 작용하는 ‘포스파티딜세린’의 수용체를 규명했다. 인지질(*용어설명 참고)의 일종인 포스파티딜세린은 세포막을 구성하는 지질 이중층 중 내부에 존재하다가 근육세포 융합과정에서 세포막의 외부로 노출되어 세포융합에 작용한다. 김인산 박사팀은 이를 인식하는 수용체를 세계 최초로 밝혀냈다. 연구진은 포스파티딜세린을 선택적으로 인식하는 수용체인 ‘스태빌린-2’라는 유전자가 근육세포의 분화 및 손상 후 근육 재형성 동안에 근육세포 융합의 효율을 조절할 수 있다는 사실을 알아냈다. 세포막을 구성하는 포스파티딜세린이 정상세포에서는 세포막의 내부에 존재하지만 세포융합(*용어설명 참고)과정에서 세포 외부로 노출된다는 점과 근육세포의 분화과정에서 다양한 포스파티딜세린의 수용체들 중에서 스태빌린-2가 다량 존재한다는 점에 착안했다. <그림 1> 스태빌린-2 유전자결핍에 의해 근육세포 분화과정 동안에 세포 융합의 감소, 정상 생쥐의 근육세포 분화(좌), 스태빌린-2 유전자결핍 생쥐의 근육세포 분화(우) 연구진은 스태빌린-2가 근육세포에서 중요한 Calcineurin/NFAT(*용어설명) 신호전달을 통해서 발현되는 것을 확인했고, 근육세포에서 스태빌린-2의 양을 증가 시키면 근육세포의 융합이 촉진된다는 연구결과를 도출했다. 이 결과를 바탕으로 스태빌린-2 유전자가 결핍된 마우스를 제작하여 근육세포에서 융합이 줄어 있음을 확인하였고, 정상 생쥐의 근육세포에 비해 손상 후 세포융합에 결함이 있는 것을 발견했다. <그림 2> 스태빌린-2 유전자결핍 생쥐에서 근육 손상 후 재형성의 결함. 정상 생쥐의 근육재형성(상), 스태빌린-2 유전자결핍 생쥐의 근육재형성(하) 연구팀은 본 연구를 통하여 포스파티딜세린 수용체인 스태빌린-2가 근육세포의 융합에 작용할 것이라는 연구진의 가설을 증명했다. 주목할 만 한 점으로 사멸세포가 아닌 살아 있는 근육세포에서 노출된 포스파티딜세린을 인식하는 수용체를 세계 최초로 규명함으로서 단순한 신호전달이 아니라 포스파티딜세린이 세포 간 융합에 직접적으로 작용한다는 기전을 밝혔다는 점에서 가치가 높은 연구결과라 할 수 있다. KIST 의공학연구소 테라그노시스연구단 김인산 박사는 “이번에 밝힌 포스파티딜세린 수용체의 기능은 근육세포 융합에 대한 정확한 기전을 밝히는 돌파구가 될 것으로 보인다”며, “본 연구의 결과를 토대로 근육세포 융합의 분자적 기전의 규명 및 세포막 융합에 작용하는 물질 규명에 더욱 힘쓸 예정”이라고 말했다. 본 연구는 미래창조과학부 지원으로 KIST 기관고유사업으로 수행되었으며, 세계적으로 권위있는 과학지인 ‘Nature Communications’에 2016년 3월 14일자 온라인판에 게재되었다. * (논문명) ‘Stabilin-2 modulates the efficiency of myoblast fusion during differentiation and muscle regeneration’ - (제1저자) 동국의대 박승윤 교수, 경북의대 윤영은 박사 - (교신저자) 한국과학기술연구원 김인산 박사, 동국의대 박승윤 교수
- 91
- 작성자테라그노시스연구단 김인산 박사팀
- 작성일2016.03.23
- 조회수23222
-
90
직물 및 의류 일체형 웨어러블 전자소자를 위한 섬유형 트랜지스터 개발
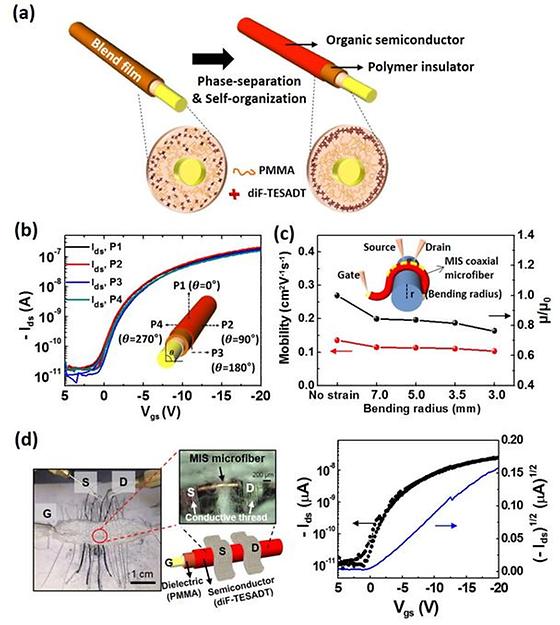
직물 및 의류 일체형 웨어러블 전자소자를 위한 섬유형 트랜지스터 개발 - 전도성 실, 면사와 함께 직조하여 옷감 일체형 전계효과 트랜지스터 구현 - 스마트 의류, 차세대 웨어러블 제품 개발에 응용 가능할 것으로 전망 최근 웨어러블 전자소자가 시대의 패러다임으로 자리 잡으면서 옷과 같은 섬유에 전자소자의 기능이 결합된 전자섬유(electronic textile)(*용어설명 참고)에 대한 연구가 활발히 진행되고 있다. 웨어러블 스마트 의류는 향후 웨어러블 시장을 주도할 것(ICT 시장조사업체 스트라베이스, 2015)으로 보인다. 섬유는 유연하고 편안하기 때문에 사람이 하루 종일 입고 다녀도 피로감을 덜 느껴 웨어러블 전자소자의 이상적인 플랫폼으로 주목받고 있다. 기존의 기술 수준은 옷감 위에 기존의 딱딱한 고체 전자소자 또는 센서 등을 단순히 붙이거나 전도성 섬유를 이용하여 소자들 사이를 연결하는 형태에 머물러 있어 섬유의 편안함을 기대할 수 없는 단계였다. 이를 개선하기 위해서는 전자소자 자체가 섬유의 특성을 유지할 수 있는 실 형태의 옷감에 삽입될 수 있는 전자소자의 개발이 필요한 상황이었다. 다양한 전자소자 중에서 트랜지스터는 센서, 디스플레이 등 전자소자 구동에 있어 기본이 되는 스위칭 소자로, 섬유형 전자소자 구현에 있어 필수적인 부품이다. 그러나 반도체와 절연막, 전도성 전극의 복잡한 다층구조로 이루어져 있어 섬유형태로 구현하는데 어려움이 있었다. 또한 기존에 보고된 섬유형 트랜지스터는 절연막과 반도체 사이의 계면접착력이 좋지 않아 외부 변형에 소자 성능이 나빠지는 단점이 있었으며, 반도체 층이 섬유의 한쪽 면에만 형성되어 있어 섬유상에 직접 직조해 넣는 데 한계가 있었다. 한국과학기술연구원(KIST, 원장 이병권) 광전소재연구단(단장 이전국) 임정아 박사팀(석사과정 김혜민 연구원)은 전도성 실 위에 1회 코팅으로 절연막과 반도체 막을 동시에 형성할 수 있는 기술을 개발하여 실 형태의 전계효과 트랜지스터(*용어설명 참고)를 구현하는데 성공하였다. 본 연구진은 용액공정이 가능한 유기반도체와 절연체 고분자의 혼합물(블렌드) 용액을 전도성 실 표면에 1회 코팅하여, 혼합물(블렌드)에서 자발적으로 상분리(*용어설명 참고)를 일으켜서, 유기반도체가 실 가장 바깥쪽 표면에 막을 형성하고 그 안쪽에는 절연체 막이 형성되어 절연막/반도체 이중층으로 감싸진 전도성 섬유 구조체를 제작하는데 성공했다. 이때 전도성 섬유는 트랜지스터의 게이트 전극(전류를 제어하는 금속접속자)으로 사용되며, 이후 소스(Source)와 드레인(Drain) 전극을 반도체 층 위에 형성하여 섬유형태의 트랜지스터를 제작하였다. 이렇게 제작된 섬유형 트랜지스터는 기존 평평한 기판에 제작되었던 유기박막 트랜지스터와 유사한 성능을 가지는 것으로 확인되었다. 임정아 박사팀이 개발한 절연막/반도체 이중층 기반 전도성 섬유 구조체는 절연막/반도체 층의 계면접착성이 우수하여 소자를 3mm 까지 접은 후에도 소자의 성능이 80% 이상 유지되는 특성을 밝혀냈다. 또한 섬유 표면 전체에 절연막/반도체가 고르게 형성되어 있어, 트랜지스터 성능이 균일하게 나옴을 알 수 있었으며, 전도성 실을 소스와 드레인 전극으로 사용하고 일반 면사와 함께 직조하여 옷감 안에 트랜지스터 소자를 직접 삽입할 수 있는 전자섬유를 제작할 수 있게 됐다. 이번 연구결과는 직조 가능한 섬유형 트랜지스터로서 기존의 평면상에 제작한 유기반도체 트랜지스터와 유사한 특성과 성능을 구현할 수 있음을 보여준 의미 있는 결과로, 차세대 웨어러블 컴퓨터, 인체신호 모니터링 기능을 가지는 스마트 의류 등 한층 똑똑해진 차세대 웨어러블 제품을 개발하는데 응용 가능할 것으로 기대된다. 또한 임정아 박사는 현재 전자섬유 연구가 세계적으로 섬유형 전자소자를 구현할 수 있는 기술을 개발하는 초기 연구단계이며, 상용화를 위해서는 전극실과의 계면안정성, 세탁 등 외부 자극에 대한 내구성을 보다 향상시키기 위한 더욱 많은 연구가 필요하다고 설명했다. 본 연구는 미래창조과학부 지원으로 KIST의 기관고유사업으로 수행되었으며, 2016년 2월 19일자 Advanced Functional Materials 온라인 판에 게재되었다. (논문명) “Metal-Insulator-Semiconductor Coaxial Microfibers Based on Self-Organization of Organic Semiconductor: Polymer Blend for Weavable Fibriform Organic Field-Effect Transistors” (DOI: http://dx.doi.org/10.1002/adfm.201504972) (제1저자) 한국과학기술연구원, 고려대학교, 김혜민 석사과정 (교신저자) 한국과학기술연구원 임정아 박사 <그림자료> <그림> (a) 유기반도체/절연체고분자 블렌드의 상분리를 이용하여 절연막/반도체 이중층 포함 전도성 섬유 구조체를 제작하는 공정 및 섬유형 트랜지스터 모식도. (b) 개발한 섬유형 트랜지스터의 섬유 표면 전방향에서의 균일한 전류-전압 특성 유지. (c) 개발한 섬유형 트랜지스터의 굽힙정도에 트랜지스터 성능 유지. (d) 전도성 실을 소스와 드레인 전극으로 사용하고 면사와 직조하여 제작한 섬유형 트랜지스터의 모습 및 동작 특성.
- 89
- 작성자광전소재연구단 임정아 박사팀
- 작성일2016.03.08
- 조회수26660
-
88
이산화탄소에서 아세톤 생산 기술 최초 개발
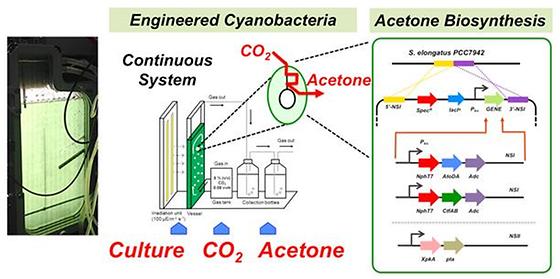
이산화탄소에서 아세톤 생산 기술 최초 개발 - 석유화학 대체로 기후변화 대응의 새로운 돌파구 열려 지구온난화의 주 원인인 이산화탄소를 활용하여 기존의 석유화학 제품을 대체할 수 있는 탄소자원화* 원천기술이 개발되었다. * 탄소자원화 : 저급 탄소 원료(이산화탄소 등)를 이용하여 다양한 탄소화합물로 전환하는 고부가화 기술 한국연구재단(이사장 정민근)은 한국과학기술연구원(KIST, 원장 이병권)과의 공동연구를 통해 인공 시아노박테리아**를 이용하여 태양광과 이산화탄소에서 아세톤***을 직접 생산할 수 있는 태양광세포공장****을 최초로 개발하였다고 밝혔다. ** 시아노박테리아 : 빛과 이산화탄소만을 이용하여 경제적으로 대량 배양이 가능하고, 식물보다 빠른 세포성장과 생산할 수 있다. *** 아세톤 : Cumeme 공법에 의해 페놀 생산 공정의 병산물로 발생하며, 아크릴 수지 및 BPA, 용제 등으로 사용된다. **** 태양광세포공장 : 미생물대사공학기술을 이용하여 인위적으로 다양한 화학제품을 대량 생산하는 공장의 개념인 ‘세포공장’에 무한한 태양광에너지를 적용하여 광합성이 가능한 세포공장 한국과학기술연구원(KIST) 우한민 박사 연구팀은 미래창조과학부 특화전문대학원 학연협력 지원사업을 지원 받아 고려대 심상준 교수와의 공동연구로 수행한 결과, 인공 시아노박테리아의 미생물을 유전자 재조합 기술 (합성생물학과 대사공학*****)로 이용하여 특정 유전자를 삽입하여 태양광과 이산화탄소가 있는 조건에서 광합성 아세톤을 만드는 생물학적 기술 개발에 성공했다. ***** 합성생물학과 대사공학 : 합성생물학은 생명과학적 이해의 바탕에 공학적 관점을 도입한 융합생물공학으로 자연계에 존재하지 않은 생물 구성요소와 시스템을 설계 및 제작하는 분야를 포함하며, 대사공학은 유용 화학제품 및 생물소재의 대량생산을 위해서 세포의 대사과정을 인위적으로 조절하는 학문임. 시아노박테리아는 빛과 이산화탄소만을 이용하여 경제적으로 대량 배양이 가능하고, 식물보다 빠른 세포성장과 생산을 할 수 있으며, 주위 환경에 따른 세포성장과 생산을 조절할 수 있다. 연구팀은 합성생물학의 기술을 통해 기존 유전자발현시스템을 재설계하고 모듈화된 발현시스템을 구축하였으며, 반응율속단계******를 우회하는 경로를 도입하여 이산화탄소에서 아세톤을 생산할 수 있도록 대사공학기법을 활용하였다. ****** 반응율속단계 : 복잡한 다단계 화학반응 (생화학 및 효소반응 포함)에서 전체 반응속도를 결정하는 가장 느린 반응단계 아세톤은 공업과 화학에서 사용되는 중요한 유기용매 및 화학 중간물질로 석유화학공정에서 이산화탄소 발생과 함께 생산된다. 그러나 이번에 개발된 태양광세포공장(인공 시아노박테리아)은 태양광과 시아노박테리아만으로 아세톤을 생산하면서도 또 다른 이산화탄소 배출이 없어 공기 중의 이산화탄소를 획기적으로 줄일 수 있는 친환경탄소자원화기술로 활용될 수 있다. ○ 석유화학제품을 친환경 바이오화학제품으로 대체할 경우 석유자원 사용량은 최대 65% 감축이 가능하고, 이산화탄소 발생량도 최대 67% 저감이 가능하다(한국과학기술기획평가원, 석유대체 친환경 바이오화학 산업정책 동향 및 R&D 이슈, 2012년). □ 우한민 박사는“이번 연구결과는 지구 온난화에 영향을 미치고 있는 이산화탄소를 순수하게 줄여 나갈 수 있는 기술로 바이오화학제품, 바이오연료 생산 등 쏠라-바이오리파이너리 기술에 적용될 수 있어 향후 기후변화에 대응하는 새로운 돌파구가 될 것”이라며 연구의 의의를 설명했다. ******* 쏠라-바이오리파이너리(Solar-biorefinery) : 오일리파이너리(Oil refinery)와 대응되는 용어로 태양광-바이오기술을 통하여 다양한 화학제품을 생산할 수 있는 기술 이 연구성과는 식물과학 분야 세계적 학술지 플랜트 바이오테크놀로지 저널(Plant Biotechnology Journal)에 2월 16일 게재되었다. <그림자료> 그림1. 유전공학기술을 이용하여 합성생물학의 모듈화전략을 도입하여 이산화탄소로부터 아세톤을 생산하는 인공 시아노박테리아를 개발하였으며, 대사공학 전략을 추가로 도입하여 시아노박테리아 내 반응율속단계를 극복하는 우수한 인공 시아노박테리아를 개발하였다. 또한 편형광반응기를 이용하여 고농도 이산화탄소로부터 아세톤을 생산하였으며, 자동으로 시아노박테리아 배지로부터 분리가 되는 반응공정을 동시에 제시하였다.
- 87
- 작성자청정에너지연구센터 우한민 박사팀
- 작성일2016.03.02
- 조회수25047
-
86
유무기 하이브리드 나노 구조 제어 기술을 이용한 산소 환원 반응 촉매 개발
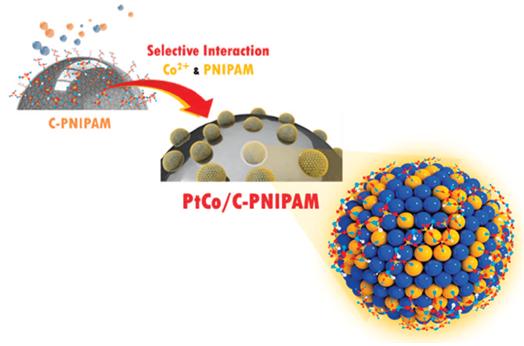
유무기 하이브리드 나노 구조 제어 기술을 이용한 산소 환원 반응 촉매 개발 - 내구성과 안정성 높은 고효율 산소 환원 반응을 일으키는 연료전지 촉매 개발 - 유무기 하이브리드 나노 기술을 통한 수소 연료전지 상용화에 기여 자동차용과 발전용, 휴대용을 포함한 고분자전해질 연료전지 시장은 2012 년 468 M$에서 2017 년 1,248 M$ 로 급격히 성장할 것으로 전망[BCC Research, 2013]된다. 하지만 현재 연료전지 전극에 고가의 백금 촉매를 대량으로 사용하고 있어 아직까지는 에너지 변환장치로서의 경제적 효용성이 낮게 평가되고 있는 실정이다. 특히, 연료전지 환원극 내 산소 환원 반응의 속도는 산화극에서의 수소 산화 반응 속도에 비해 매우 느리기 때문에 산화극 촉매 대비 2 배 이상의 백금 촉매가 사용되어야만 한다. 따라서 저가의 고활성 산소 환원 반응 촉매의 개발이 필요했고, 수소 연료전지로부터의 안정적인 전력 생산을 위해 높은 전기화학적 활성뿐만 아니라 장기 내구성 역시 갖춰야하는 촉매를 개발하는 것이 매우 어려운 과제였다. 지난 10 여 년 동안, 고가의 백금 촉매 사용량을 저감하면서 동시에 촉매의 산소 환원 반응 활성을 극대화기 위해 니켈 (Ni), 코발트 (Co), 철 (Fe)과 같은 3d 전이금속을 백금과 합금시키는 연구가 활발히 진행되었다. 나노 기술의 발달과 함께 연료전지 환원극에서의 산소 환원 반응을 위한 고활성 백금계 합금 나노 입자를 제조할 수 있었으나, 쉽게 산화되는 3d 전이금속의 물리적 특성에 의해 이론적으로 가능한 촉매 활성을 충분히 내지 못하였고, 동시에 장기 내구성까지 약화되는 어려움이 있었다. 실제로 제조된 백금-전이금속 합금 나노 입자가 공기(산소) 또는 수분에 노출되면 니켈, 코발트, 철 등의 3d 전이금속 원자를 가진 나노 촉매 입자 표면이 즉각적으로 산화되어 금속산화물을 형성하여 산소 환원 반응 활성은 이론적인 값보다 상대적으로 낮아지게 된다. 또한 나노 촉매 입자 표면에서 공기 및 수분에 의해 이미 산화된 3d 전이금속 원자는 연료전지가 구동되는 높은 전압 및 낮은 pH 환경에서 쉽게 녹아내려 촉매 성능을 급격하게 떨어뜨렸다. <그림 1> KIST 유성종 박사팀은 기존 백금-전이금속 합금 촉매가 가진 근본적인 단점을 보완하기 위해, 아미드(amide)(*용어설명 참조)기를 가진 고분자를 이용하여 나노 촉매 입자 표면에 존재하는 3d 전이금속 원자를 선택적으로 기능화 함으로써 산소 환원 반응 활성 및 장기 내구성이 극대화된 연료전지 촉매를 개발했다. <그림2> 나노 촉매 입자 표면에서 선택적으로 코발트 (Co)-질소 (N) 결합을 형성하게 함으로써 코발트에서 백금으로 전달되는 전자 이동을 보다 원활하게 하여 반응 활성 사이트인 백금의 전자 구조를 산소 환원 반응에 보다 유리하게 변형시켜 촉매 활성을 기존 백금계 합금 촉매 대비 약 2배가량 향상시켰고, 나노 입자의 선택적 고분자 기능화에 의한 안정화(passivation) 효과가 나타남으로써 코발트 원자의 소멸(dissolution)을 방지하여 촉매 내구성이 약 4배 정도 향상되었다. <그림 3> 인도 방갈로르에 소재한 KIST 한-인도협력센터 이승철 박사연구팀은 인도의 연구진과 함께 제일원리 전자구조계산 기법(*용어설명 참조)을 통해 순수한 금속상태에서는 코발트 (Co)-질소(N) 결합이 백금-질소결합보다 약하지만 코발트와 백금이 1:1로 섞여 합금을 만드는 경우 백금-질소결합보다 코발트-질소결합이 더 강할 수 있다는 것을 이론적으로 예측하였다. 그리고 이런 결합강도의 역전현상은 코발트에서 백금으로 전하가 전달됨으로써 순수한 코발트와는 다른 전기적, 자기적 특성을 보이기 때문이라고 설명하였다. KIST 유성종 박사는 “유무기 하이브리드 나노 구조 제어 기술을 통해, 백금계 산소환원반응 촉매가 가지고 있는 치명적인 단점을 효과적으로 보완한 연구라는 관점에서 기존의 연구와 큰 차별성을 가지고 있다”며, “이번 연구로 수소 연료전지의 상용화를 한 발 앞당겼다는데 의미가 있다”고 말했다. 또한 KIST 한-인도협력센터 이승철 박사는 “본 연구를 통해 백금에 비해 매우 저렴한 자성금속을 촉매로 활용할 수 있어 저렴한 생산비로 높은 반응성과 안정성을 가진 촉매를 개발할 수 있는 가능성을 열었다는 점도 중요하다”고 말했다. 본 연구는 KIST 기관고유 연구사업, 미래창조과학부의 글로벌프론티어사업, 한국연구재단 중견연구자지원사업과 국가과학기술위원회 CAP과제를 통해 수행되었으며 연구결과는 세계적 권위를 자랑하는 Nature의 자매지로서 에너지 및 나노 분야의 국제 저명 학술지인 NPG Asia Materials (IF: 10.118)에 1월 게재되었고, 연구의 우수성을 인정받아 이달의 Top 10 Articles (most downloaded articles)에 선정되었다. 더욱이, 해당 연구결과는 국내특허 출원 (출원번호:2015-0014254) 및 해외 특허 출원도 (출원번호:14/918486) 진행 중에 있다.
- 85
- 작성자연료전지연구센터 유성종 박사팀
- 작성일2016.02.29
- 조회수26267
-
84
간단한 제조공정으로 다기능 그래핀 나노복합구조 양자점 합성 기술 개발
간단한 제조공정으로 다기능 그래핀 나노복합구조 양자점 합성 기술 개발 - 고효율 유기 태양전지 소자 기술 응용 적용 - 유기태양전지 효율 증가, 비용 절감 및 안전성 획기적 개선으로 상용화에 한 발 다가서 태양광을 전기 에너지로 바꾸는 태양전지는 화석 에너지의 고갈과 청정 에너지원의 필요성이 부각되면서 차세대 대체 에너지원으로서 각광 받고 있다. 현재 태양전지는 실리콘계 태양전지가 주로 생산되고 있으나 복잡한 제작공정 및 높은 재료 가격으로 인하여 경제성 확보에 어려움을 겪고 있다. 이에 반해, 유기태양전지는 기존 실리콘계 태양전지와 달리 가공이 쉽고 재료가 다양하며, 가격 또한 저렴하여 경제성이 높다. 그러나 상대적으로 빛을 전기로 바꾸는 광전 변환 효율이 낮고 오래 사용할 경우 안정성이 떨어져 상용화에 어려움이 있었다. 국내 연구진이 기능화된 탄소기반 양자점 단일층을 효과적으로 도입하여 유기태양전지의 안정성 및 광전 변환 효율을 획기적으로 개선한 태양전지를 개발했다. 이러한 이점을 통해 태양전지의 전기적인 성능과 다기능한 역할로 기존보다 약 17.8%이상 효율을 증가함과 동시에 광 에너지 전환 효율(power conversion efficiency: PEC)은 최대 10.3%의 효율을 얻었고, 안정성도 개선됨을 확인하였다. 그래핀 표면에 기능화 형성을 위한 합성을 하였고, 이를 통해, 유기용매 분산도를 높이고 고분자(PEIE)층과 더욱 강한 전기적 결합으로 인해 박막 형성 시 균일한 단일층을 형성할 수 있다. 기존의 금속산화물에 전기전도도가 우수한 그래핀을 껍질로써 감싸고 이를 화학적으로 기능화를 시켜주게 되면 유기용매 분산도가 향상되고, 표면 개질 고분자 층위에 코팅하게 되면 거칠기(roughness)또한 줄어들게 되므로 이는 균일한 박막이 형성되는데 도움을 준다. 이는 ITO전극에 표면개질 고분자만 존재했을 때 보다 일함수가 낮아져 생성된 전하가 빠르게 이동할 수 있다. 한국과학기술연구원(KIST) 전북분원(분원장 김준경) 복합소재기술연구소 양자응용복합소재센터 손동익 박사 연구팀은 유기태양전지의 표면 개질 고분자 층(PEIE) 표면 위에 ‘기능화된 산화아연-그래핀 양자점’을 수 나노미터 두께인 단일층으로 처리하여, 광전환 효율을 증대시키고, 소자의 안정성을 강화한 유무기 하이브리드 구조의 유기태양전지를 개발했다. 일반적으로 유기태양전지에서 태양광을 흡수하여 전자(Electron)와 정공(Hole)을 형성하는 광활성층(Active layer)이라 불리는 유기물층 (PTB7 혹은 PTB7-Th 고분자 물질)은 태양광을 받아 전자를 내놓는 ‘전자주게물질’(Donor)과 전자를 받아서 전극으로 전달해주는 ‘전자받게물질’ (Acceptor; PCBM: 탄소나노물질)의 혼합층 (탄소복합구조)으로 이루어져 있다. 하지만, 태양전지의 효율 및 안정성을 보장하기 위해서는 몇 가지의 원활한 소자구동을 위한 전자수송층(eletron transport layer), 정공수송층(hole transport layer), 전자주입층(eletron injection layer), 정공주입층(hole imjection layer) 등이 도입되어야한다. 연구팀은 또한 기존의 표면 개질 고분자층(PEIE)을 사용한 구조에서는 ITO(Indium tin oxide:투명전극)전극의 일함수를 낮춰주고 태양전지의 전기적 성능을 증가시켜주는 역할을 해주는 데에만 그쳤으나, 광활성층에서 나오는 전하를 효과적으로 이동시켜줄 수 있도록 전자수송층을 도입하였고, 기존에 사용된 자외선 영역의 파장을 가지는 넓은 밴드갭의 금속 산화물 나노입자(ZnO)는 전자 수송층으로만 사용했었기 때문에 효율을 향상시키기에는 많은 제약이 있었다. 이러한 문제를 해결하기 위해서 기존의 금속산화물에 전기전도도가 우수한 그래핀을 껍질로써 감싸고 이를 화학적으로 기능화를 시켜주게 되면 유기용매 분산도가 향상되고, 도 좋아지며 표면 개질 고분자 층위에 코팅하게 되면 거칠기(roughness)또한 줄어들게 되므로 이는 균일한 박막이 형성되는데 도움을 준다. 이는 ITO전극에 표면개질 고분자만 존재했을 때 보다 일함수가 낮아져 생성된 전하가 빠르게 이동할 수 있다는 것을 의미한다. 이러한 이점을 통해 태양전지의 전기적인 성능과 다기능한 역할로 기존보다 약 17.8%이상 효율을 증가함과 동시에 안정성도 개선됨을 확인하였다. ※ 밴드갭 : 전자가 존재하는 에너지 레벨과 전자가 존재하지 않는 에너지 레벨의 사이의 차이 ※ 일함수 : 특정한 고체 표면에서 한 개의 전자를 외부로 빼내는데 필요 <그림 1> 개발된 ‘기능화된 산화아연-그래핀 양자점 단일층’은 단순한 용액공정을 통하여 쉽고 빠르게 형성할 수 있고, 기존의 산화아연-그래핀 양자점보다 우수한 단일층 형성을 보이며 효과적으로 광활성층에서 생성된 전자가 전극으로 원활하게 이동하는 것에 도움을 주게 되어 태양전지의 광전 변환 효율의 증대를 가져 오게 된다. <그림 2> 기존 그래핀 표면에는 존재하지 않는 ?NH 또는 ?NR 기능기 (Yellow: ZnO, Black: Carbon, Red: Oxygen, Grey: Hydrogen, Blue: Nitrogen, Green: Alkyl group(-C7H15))가 옥틸아민(Octylamine)을 통해 그래핀 표면에 형성 됨으로써 유기용매 분산도를 높이고 PEIE층과 더욱 강한 전기적 결합으로 인해 박막 형성 시 균일한 단일층을 형성하고 이를 통해 증가된 태양전지의 효율과 안정성에 기여 하였다. <그림 3> (a)에서 볼수 있듯, 기능화된 산화아연-그래핀 양자점을 소자로 제작하기 위해 단일층으로 형성시킨 역구조 솔라셀 구조로 형성내며, (b)와 같이 솔라셀 소자에서 기능화된 산화아연-그래핀 양자점이 단일층으로 형성된 형상을 투과전자현미경(Transmission Electron Microscope: TEM)으로 단일층 구조체의 단면을 측정하여 확인하였다. 이 구조체를 통해서 유기용매 분산도도 좋아지며 표면 개질 고분자 층위에 코팅하게 되면 거칠기(roughness)또한 줄어들게 되고 이는 태양전지소자의 활성 폴리머 물질이 균일한 박막이 형성되는데 도움을 주게 되고, 이는 ITO전극에 표면개질 고분자(PEIE)만 존재했을 때 보다 일함수가 낮아져 생성된 전하가 빠르게 이동할 수 있다는 것을 의미한다. 이러한 이점을 통해 태양전지의 전기적인 성능과 다기능한 역할로 기존보다 레퍼런스 대비 약 17.8%이상 효율을 증가함과 동시에 안정성도 개선됨을 확인하였다. <그림 4> 이러한 효과로 기능화된 산화아연 그래핀 양자점 단일층을 이용하여 제작된 역구조 유기태양전지의 특성은 태양전지소자의 광 에너지 전환 효율(power conversion efficiency: PEC)은 최대 10.3% 이상 증가 하였고, 양자점 단일층에 의해 형성된 역구조 유기태양전지는 대기와 접촉에서 안정성 증가 확보가 가능하므로, 기능화된 양자점 없는 소자와 비교해서 효율의 안정성이 94%까지 유지되는 것을 보여주는 데이터이다. KIST 손동익 박사는 “기능화된 산화아연-나노카본 양자점을 이용하여 기존 전자수송층 뿐만 아니라, 다양한 기능의 특성을 통해서 광에너지 전환 효율을 향상시키고, 솔라셀 폴리머 물질과의 계면 인터페이스 또한 우수하여 유기태양전지의 내구성을 획기적으로 개선시킨다”며, “후속으로 연구 중인 나노카본을 기반으로 한 금속 물질 복합구조 양자점을 사용한다면 유기태양전지의 상업화에 크게 기여할 것으로 보인다”고 말했다. 본 연구는 미래창조과학부가 지원하는 KIST 기관고유연구사업으로 수행되었으며, 이번 연구 성과는 에너지재료 분야의 권위지인 나노에너지(Nano energy)에 "Enhanced Photovoltaic Performance of Inverted Polymer Solar Cells utilizing Versatile Chemically Functionalized ZnO@graphene Quantum dot Monolayer"의 제목으로 2016년 1월 14일에 온라인판으로 게재되었다.
- 83
- 작성자전북분원 복합소재기술연구소 양자응용복합소재센터 손동익 박사 연구팀
- 작성일2016.02.23
- 조회수17249
-
82
심장질환, 차세대 염증억제 약물방출 스텐트로 해결한다
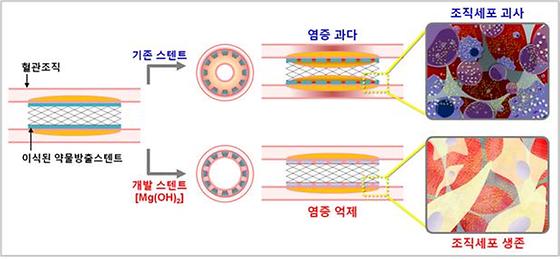
심장질환, 차세대 염증억제 약물방출 스텐트로 해결한다 - 무독성 세라믹 나노입자를 이용한 비약물 염증억제 시스템 개발 - 획기적 염증 억제와 재협착을 방지하는 관상동맥용 약물방출 고성능 나노표면 스텐트 개발 전 세계 사망 원인의 1위가 심장혈관 질환으로, 2012년 기준 전체 사망자 수의 약 31%인 1,750만 여명이 심장혈관질환으로 목숨을 잃었으며 이 중 관상동맥질환으로 인한 사망자 수는 740만 명에 달한다. 국내에서의도 심장질환은 암에 이은 2번째로 높은 사망원인으로 매년 환자수가 꾸준히 증가하고 있으며, 2012년 기준 국내의 관상동맥질환 환자 수는 2003년 50만명에 비해 58.4%가 증가된 79만명으로 집계되었다. 한국과학기술연구원(KIST, 원장 이병권) 생체재료연구단 한동근 박사 연구팀(이하 연구팀)은 기존의 관상동맥용 약물방출 스텐트(drug-eluting stent, DES)의 표면에 pH 중화 기능을 가진 수산화마그네슘 무독성 세라믹입자를 코팅하여 염증을 획기적으로 억제하고 재협착을 방지하는 심장 관상동맥용 약물방출 스텐트를 세계 최초로 개발했다. 초기 금속스텐트(bare metal stent, BMS)는 비흡수성 금속소재로 제작되어 스텐트 삽입술 후 혈관 평활근세포의 증식에 의한 재협착의 부작용을 보였다. 이후 약물이 코팅된 약물방출 스텐트가 개발되어 재협착은 기존 금속 스텐트에 비해서 현저하게 줄었으나, 약물방출 스텐트 표면에 코팅된 고분자와 약물로 인해서 수년 후혈액이 응고되는 후기 혈전증 문제가 새롭게 제기되었다. 따라서 금속 스텐트와 약물방출 스텐트의 문제점을 모두 해결한 이상적인 스텐트는 개발되지 않은 상황이었다. 일반적으로 스텐트 이식 후 시간이 지남에 따라 코팅된 생분해성 고분자가 분해되면서 분해산물인 산성 단량체(작은 단위체)가 생성되는데, 이로 인해 pH가 산성화되면서 혈관 주변 조직세포의 괴사가 일어나고 그 결과 염증이 발생하여 재협착이 가속화된다. KIST 한동근 박사 연구팀은 이러한 혈관 내 염증을 현저히 억제하여 재협착을 방지하는 심근경색 치료용 차세대 관상동맥 약물방출 스텐트를 개발하였다. 본 연구팀은 제산제나 연하제 등에 이용되고 있는 염기성 수산화마그네슘 세라믹입자[Mg(OH)2]의 pH 중화 효과에 주목하였다. 염기성 수산화마그네슘 세라믹 입자를 첨가했을 경우, 산성화된 혈관 내 환경의 pH가 중화되고, 조직세포가 그대로 생존하여 괴사를 막아 염증을 억제함을 밝혀냈다. 기존에 염증억제를 위한 대표적인 약물인 ‘덱사메타손’을 첨가한 스텐트가 연구되었지만 약물의 심한 부작용으로 인하여 상품화되지 못했다. 대조적으로 생체적합성 세라믹 입자는 인체에 무해하고, 약물과 다르게 생체 내에서 분해되어 오히려 이로운 마그네슘 이온이 되는 장점을 가지고 있다. 또한 이러한 기능을 가진 수산화마그네슘 세라믹입자의 표면을 항염증 효과를 지닌 지방산과 생분해성 고분자로 개질함으로써 pH 중화뿐만 아니라 코팅 매트릭스 고분자의 기계적 물성 개선에도 효과를 보이는 수산화마그네슘 비약물 나노입자를 개발하였다. 연구팀은 개발된 비 약물 나노입자가 함유된 약물방출 스텐트의 염증 억제 및 혈관 내 재협착 방지 효과를 생체 내 검증하기 위해 전남대병원 순환기내과 정명호 교수팀과 공동 연구하여 돼지를 이용한 동물실험을 실시하였다. 그 결과, 기존 스텐트에 비해 염증이 90%이상 감소하였고, 이로 인해 협착률도 3배 이상 감소하였다. 개발된 염증억제 기술은 스텐트뿐만 아니라 생분해성 고분자를 이용한 거의 모든 의료용 이식소재에 확대 적용할 수 있을 것으로 기대된다. 협심증 및 심근경색 환자의 심장 관상동맥이 막히거나 좁아졌을 때 시술하는 약물방출 스텐트 삽입술은 2014년 국내 기준 약 3천억원 이상에 육박하는 시술이 시행되었다. 국내 관상동맥용 스텐트 시장의 성장률은 식생활의 서구화 및 고지혈증과 같은 심장 질환의 증가로 급속도로 상승하고 있다. 따라서 스텐트 원천기술 확보 및 개발은 노령화 사회에 대응하는 미래첨단융합기술로 발전할 전망이다. 스텐트 제품의 경우 다국적 기업의 기술 및 상품 수입에 따른 기술의 종속화 이전에 차세대 핵심 기술이 확보되면 이를 통해 국제 경쟁에서 우위 선점이 가능하다. 연구팀은 “2015년 현재 혈관 스텐트의 세계 시장은 연간 10조원, 국내 시장은 4,000억원으로 추정되지만 스텐트는 우리나라 수입 의료용품 중 그간 1위 품목으로 수입 의존도가 높기 때문에 선진국과의 기술 격차를 좁히고, 국산화를 위한 지속적인 원천기술 개발과 지원이 필요하다”고 강조했다. 또한, 연구팀은 “이번에 개발된 약물방출제어 나노표면 스텐트는 차세대 미래형 스텐트 국산화 및 실용화에 크게 기여를 할 것이다”라고 밝혔다. 연구팀은 2008년부터 현재까지 관상동맥용 약물방출 스텐트 개발에 관한 미래창조과학부의 미래유망 융합기술 파이오니어사업으로 진행되었으며, 사업 수행기간 중 염증억제 기술을 포함한 원천 핵심기술을 연구·개발하여 다수의 국내외 특허등록을 받았으며, Small(IF=8.368) 등 국제 저명학술지에 논문을 게재한 바 있다. 또한 본 연구 결과는 “심장 관상동맥용 약물방출 스텐트 표면개질” 기술로 2015년 ㈜바이오알파(유현승 대표)에 기술 이전하여 고성능 나노표면 제어 차세대 약물방출 스텐트의 실용화 및 국산화가 진행 중이다. 향후 추가 전임상 동물실험 및 임상실험은 전남대학교 심장센터와 진행할 예정이며, 이 기술은 앞으로 2년 이내에 상품화가 가능할 것으로 전망된다. <그림자료> ○ 개발된 약물방출 스텐트의 염증억제 작용기전을 나타낸 그림. ○ 조직세포가 괴사되고 염증이 발생하는 기존 스텐트와 대조적으로, 약물방출 스텐트에 약물과 함께 코팅에 사용된 염기성 수산화마그네슘 세라믹 입자가 생분해성 고분자가 분해되면서 생성되는 산성 단량체에 의해 낮은 pH로 산성화된 주변 환경을 중화시킴으로써 조직세포의 괴사를 막고 염증을 효과적으로 억제하는 것을 확인함. ○ pH 중화 나노입자의 제조방법 및 특성을 나타낸 그림. ○ 자체의 pH 중화효과를 가지고 있는 수산화마그네슘 세라믹입자에 항염증 효과를 보이는 것으로 알려진 지방산인 리시놀레산(ricinoleic acid, RA)과 생분해성 고분자로 표면을 개질하여 최종적으로 pH 중화효과 뿐만 아니라 기계적 물성향상 효과도 보이는 수산화마그네슘 세라믹입자를 개발함. 이러한 표면개질된 나노입자도 pH 중화효과뿐만 아니라 세포를 죽이지 않고 염증도 현저하게 저하시킴을 확인함. ○ 기존의 약물방출 스텐트와 비교하여, 수산화마그네슘 세라믹 나노입자를 포함한 개발 스텐트의 우수한 염증억제 효과와 현저히 낮은 재협착률을 보여주는 4주 돼지 동물실험 결과임. ○ 개발된 스텐트가 기존 스텐트에 비해 90% 이상 염증이 감소하였고, 3배 이상의 협착률 감소를 보임. 이 결과로부터 기존 스텐트에 비해 개발 스텐트에서 염증이 거의 일어나지 않고 재협착 발생도 대폭 감소하는 것을 재확인할 수 있음.
- 81
- 작성자생체재료연구단 한동근 박사 연구팀
- 작성일2016.02.05
- 조회수26830
-
80
항공우주 복합소재용 고내열 수지 제조 원천기술 개발
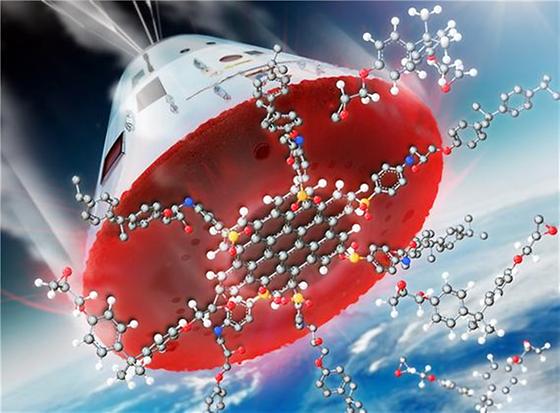
항공우주 복합소재용 고내열 수지 제조 원천기술 개발 - 산화 그래핀의 기능화를 통해 고내열 고강도 고분자 수지 제조 원천기술 개발 - 고내열 수지와 고강도 탄소섬유의 복합화를 통해 항공우주용 초고강도 탄소복합소재 상용화를 앞당기는 혁신적 기술 개발 전 세계적으로 자동차, 우주항공 등에서 경량화를 통한 연비 향상과 이산화탄소 배출량을 감소시키기 위하여 탄소복합소재의 활용에 관한 연구가 활발히 진행되고 있다. 국내 기업들은 탄소섬유의 저가화 및 고강도화에 대한 투자와 생산을 늘리고 있으나, 탄소복합소재의 다양한 응용범위에 맞는 에폭시 수지의 개발은 미진한 상황이었다. 한국과학기술연구원(KIST, 원장 이병권) 전북분원(분원장 김준경) 복합소재기술연구소 탄소융합소재연구센터 고문주 박사팀은 산화 그래핀을 화학적 방법을 통해 기능화하고 저가의 범용에폭시와 혼합하여 고내열 고강도 성능을 구현하는 원천 기술을 개발했다. 탄소섬유와 고분자수지의 복합화로 얻어진 탄소복합소재는 비행기, 자동차, 자전거, 로켓 등의 경량화를 시킬 수 있어 연비향상 뿐 아니라 지구온난화의 주요 원인인 이산화탄소 배출을 줄일 수 있을 것으로 기대 된다. 고분자 수지 중 에폭시 수지는 탄소복합소재의 구조를 안정시키는 역할을 담당하는 물질로서 탄소복합소재의 응용분야를 확대하기 위해서는 다양한 종류의 에폭시 수지가 요구되고 있다. 지금까지 항공우주용 고내열 에폭시 수지의 경우는 전량 선진국에서 수입한 고가의 특수 에폭시를 사용해 왔으나, 국내연구진이 저가의 범용에폭시 수지에 산화 그래핀 유도체를 첨가하여 고내열성능을 구현하는데 성공했다. KIST 고문주 박사 팀은 에폭시 수지의 경화에 사용되는 분자를 화학적으로 도입한 기능화 산화 그래핀은 저가의 범용 에폭시 수지와 혼합 사용하여도, 고내열 성능과 고강도 특성을 얻을 수 있음을 밝혀냈다. 고문주 박사팀은 산화그래핀에 에폭시 수지와 가교결합을 형성 할 수 있는 아민 그룹(amine group)을 도입하여, 산화 그래핀 주위에 존재하는 다량의 아민 그룹이 에폭시 수지와 결합하여 많은 가교결합을 통해 가교 밀도가 약 240% 향상되는 것을 밝혀냈다. 연구팀은 에폭시 수지와 가교결합을 하고 있는 산화 그래핀은 에폭시 수지의 강도와 열적 성질을 크게 향상시켰다고 밝혔다. 본 연구결과는 고내열성능을 요구하는 분야로의 탄소복합소재 상용화를 앞당길 수 있을 것으로 보인다. 또한, 고성능의 에폭시 수지의 합성설계에 필요한 원천기술을 확보함으로서, 국내의 탄소섬유와 에폭시 수지 분야 연구불균형 해소에 크게 기여할 것으로 보인다. 이번 연구는 KIST 기관고유연구사업에서 지원되었으며, 연구 결과는 영국왕립화학회에서 발간하는 고분자분야의 권위지인 Polymer Chemistry 표지논문으로 12월 16일자 게재되었다. * (논문명) "Enhancement of the crosslink density, glass transition temperature, and strength of epoxy resin by using functionalized graphene oxide co-curing agents" <그림자료> <그림 1> 기능화 산화그래핀을 이용한 고내열 수지와 이를 이용한 항공우주용 초고강도 복합소재의 모식도
- 79
- 작성자복합소재기술연구소 탄소융합소재연구센터 고문주 박사팀
- 작성일2016.01.14
- 조회수20126
-
78
몸에서 녹는 금속 나사의 뼈 생성 원리 밝혀
몸에서 녹는 금속 나사의 뼈 생성 원리 밝혀 - 생체 분해성 금속 소재의 인체 내 분해 메카니즘 규명 - 산학연병 공동연구 결과로 국내 의공학 연구의 새로운 모델 제시 빙판길 낙상사고가 급증하는 계절, 낙상을 포함하여 사고로 인해 골절 환자가 증가하고 있다. 골절 부상은 보통 부러진 뼈를 고정하는 장치를 사용하여 수술하게 되는데, 몸속에 남아있는 금속 임플란트로 인해 우리는 부작용을 겪거나 불편함을 경험하게 된다. 국내 산학연병 공동연구진이 이러한 문제를 해결할 수 있는 생분해성 금속 정형외과 임플란트를 개발하였다. 생분해성 금속은 체내 이식 후 일정 기간(1-2년)이 경과되면 분해되어 체내에서 소멸되는 소재로서, 이러한 소재를 이용하여 의료기기를 제조하면 손상된 인체조직이 복원된 후 이식된 의료기기를 제거하는 2차 시술을 생략할 수 있다. 한국과학기술연구원(KIST, 원장 이병권) 의공학연구소 생체재료연구단 김유찬 박사팀은 인체 구성원소를 이용하여 제조된 생분해성 금속이 실제로 환자에게 장기간 이식 되어도 아무런 문제가 없다는 것을 최첨단 분석기법을 이용하여 과학적으로 증명하였다. 연구팀은 향후 이 소재를 이용한 다양한 혁신 의료용 임플란트가 개발될 수 있는 결과를 발표하였다. 특히 이 생분해성 금속은 골절치료 분야에 새로운 장을 열 것으로 기대된다. 본 연구는 생분해성 마그네슘 합금이 체내에서 녹는 과정을 보여주는 세계 최초의 연구결과이다. 연구진은 기존의 염색기법과는 다른 빌라누에바(villanueva) 골염색법이라는 새로운 분석기법과 재료연구에 사용되는 전자현미경을 이용하여 쉽게 관찰할 수 없었던 생체분해성 금속과 인체조직간 계면에서 일어나는 연속적 분해거동을 세포에서 원자단위까지 계층적인 분석을 통해 밝혀내었다. 특히, 골 염색으로 관찰한 생물학적 영역에서의 분석에 그쳤던 기존의 연구결과와는 달리, 생분해성 금속소재영역과 그 경계까지의 연속적인 변화거동을 재료분석 기법인 전자현미경을 사용하여 동시에 관찰했다. 생분해성 금속이 체내에서 녹으면서 신생골을 형성시켜 골절의 치료에 도움을 주는 현상을 시간의 흐름에 따라 확인할 수 있었다. 연구진이 개발한 마그네슘 임플란트는 아주대학교 병원에서 53개의 사례에 이식되어 각각 6개월에서 12개월간 관찰하여 어떠한 부작용도 없이 치료를 완료하였으며, 이를 통해 판매허가를 획득한 바 있다. 본 연구에서는 이 과정에서 생분해성 마그네슘이 녹으면서 주변골과 유사한 조직을 만들고 이들 주변에 뼈조직을 형성하는 세포를 불러들여 최종적으로 신생골로 변화시키는 과정을 확인했다. 이 같은 결과는 장기간 임상결과를 통해, 치료효과에 대한 과학적인 근거를 바탕으로 인체에 대한 안정성 및 기능성을 동시에 증명한 결과로서 이후 생분해성 금속소재의 사용에 대한 인식을 전환시켜 많은 영역에 활용될 수 있는 가능성을 제시하고 있다. 김유찬 박사는 “본 기술은 KIST, U&i(주), 서울아산병원, 아주대병원, 국민대학교 등 산학 연병의 컨소시엄으로 구성하여 기초연구에서부터 임상결과까지 전 과정을 고찰하여 얻어진 융합연구로서, 의공학 연구에 새로운 모델을 제시한 의미 있는 결과이다. 하지만, 재료물성의 한계로 수지부와 같은 비교적 응력을 덜 받는 부위에만 사용하고 있고, 향후 강도 및 연신율이 향상된 마그네슘 함금개발이 반드시 진행되어야 한다. 이에 본 연구결과를 바탕으로 골 전반에 걸쳐 사용할 수 있는 새로운 합금이 개발된다면 연 30~40조원에 해당하는 시장이 창출될 것으로 예상되며 이와 같은 시장을 선점하기 위해서는 국가적 지원이 절실히 필요하다”고 밝혔다. 본 연구는 KIST 의공학연구소 플래그쉽 연구사업과 서울시 RNBD사업의 지원으로 수행되었으며, 연구결과는 세계적 학술지인 미국국립과학원회보(Proceedings of the National Academy of Sciences; PNAS) 1월 4일자 온라인판에 게재되었다. * (논문명) Long-term clinical study and multiscale analysis of in vivo biodegradation mechanism of Mg alloy - (공동 제1저자) 국민대학교 이지욱 연구교수, 한국과학기술연구원 한형섭 연구원, 아주대학교병원 한경진 교수 - (공동 교신저자) 한국과학기술연구원 김유찬 책임연구원, 서울아산병원 이강식 박사 <그림자료> <그림 1> 본 연구에서 계층적 분석을 한 조직학적 사진 및 전자현미경사진. 토끼 대퇴골과에 마그네슘 합금 임플란트를 식립하고 8주 후가 되면 최초 임플란트가 체내에서 녹으면서 석회화층과 신생골이 생성되고 있는 것을 관찰 할 수 있다. <그림2> 마그네슘 합금 임플란트과 신생골 계면에 대한 전자현미경 분석. (A) 마그네슘과 산소가 많은 영역I, 칼슘과 인이 많은 영역II, III, V, 탄소가 많은 영역IV로 구분된다. (B) 각 영역에 대한 미세구조의 변화를 보여주는 사진으로, 영역 I, 영역 II는 비정질구조, 영역 II’, 영역 III은 결정질 구조를 나타낸다. (C) 각 영역에 대한 (마그네슘+칼슘) / 인의 비율, 마그네슘 (%), 칼슘 (%), 인 (%)의 성분변화. <그림3> 식립 기간에 따른 마그네슘 합금 임플란트 계면의 villanueva 염색된 골조직사진이며 (A)는 8주 (B)는 16주 그리고 (C)는 26주를 나타낸다. (A, i) 식립 후 8주에서 마그네슘합금의 녹는 모습을 형광 저배율에서 찍은 사진이며 , (B, i) 식립 후 16주, (C, i)는 26주 후의 저배율 사진이다. (A, ii) 식립 후 8주에서 뼈의 형성 모습을 형광-고배율에서 찍은 사진이며, (B, ii) 식립 후 16주, (C, ii)는 26주 후의 고배배율 사진이다. 그리고 (A, iii) 식립 후 8주에서 뼈의 형성 모습을 자영광-고배율에서 찍은 사진이며, (B, iii) 식립 후 16주, (C, iii)는 26주 후의 고배배율 사진이다. (A, i), (B, i), (C, i)의 주황색 실선은 원래의 임플란트 표면을 나타내며, 파란색의 점선은 각 식립시간에서의 임플란트 중앙부를 나타낸다. <그림4> 마그네슘 이식 1년 후, 완전히 녹으면서 뼈가 치유된 임상결과이다. (A) 요골 골절에 이식한 마그네슘합금 임플란트(MI)와 주상골 골절 부위에 스테인레스 임플란트(SI)를 이식 후, 1년 후 환자의 왼쪽 X-ray 사진이다. (B) 시술 경과에 따른 X-ray 사진을 나타낸다. (i) 시술 전 요골 골절과 주상골 골절 (ii) 시술 직후 요골 골절에 식립한 MI (노란색 화살표)와 주상골 골절부에 이식된 SI, (iii) 시술 6개월 후 요골 골절에 이식된 MI와 주상골 골절부에 식립한 SI, (iv) 시술 12개월 후 경과. (C) 시술 경과에 따른 MI의 변화를 설명하는 모식도. 빨간색 화살표는 요골 골절, 백색 화살표는 주상골 골절, 노란색 화살표는 MI를 나타낸다.
- 77
- 작성자생체재료연구단 김유찬 박사팀
- 작성일2016.01.14
- 조회수27797
-
76
웨어러블 바이오센서 핵심 기술 개발
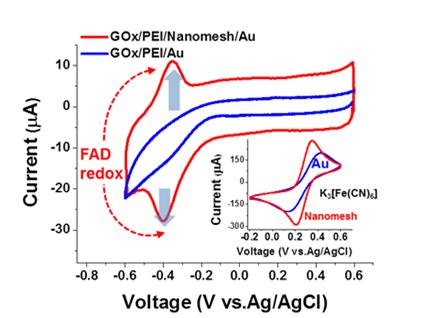
웨어러블 바이오센서 핵심 기술 개발 - 나노 소재와 바이오 물질을 이용하여 효소와 전자를 직접 주고받는 방식의 고 생체 안정성, 고선택성, 고민감도 바이오센서 기술 개발 - 유연집적소자 구현이 가능하고 다양한 효소에 적용 가능한 플랫폼 기술로 차세대 헬스케어용 웨어러블 디바이스에 활용 가능 최근 신체에 착용하거나 부착하여 생체 정보를 모니터링하고 건강을 관리할 수 있는 웨어러블 디바이스에 대한 관심이 급격히 증가하고 있다. 지금까지개발된 웨어러블 센서는 주로 인체의 움직임이나 물리적인 정보들을 모니터링하는 것이 주류였다. 인체에 부착하여 눈물, 땀 등 생체 용액을 분석하여 건강지표와 관련 있는 화학적인 정보를 얻을 수 있는 웨어러블 센싱 플랫폼 기술은 상대적으로 그 개발 속도가 뒤쳐졌다. 이는 웨어러블 바이오센서의 경우 선택성과 민감도뿐만 아니라 신체 안정성과 기계적 유연성이 동시에 만족해야 하므로 이를 구현하는 데 기술적으로 어려움이 있었기 때문이다. 한국과학기술연구원(KIST, 원장 이병권)은 스핀융합연구단 이현정 박사팀이 “나노 소재와 바이오 물질을 이용하여 인체 안정성이 높고 선택성과 민감도가 뛰어난 유연 바이오 센싱 플랫폼 기술을 개발했다”고 밝혔다. 눈물, 땀, 타액 등의 생체 용액은 건강 상태와 관련된 생체 지표들(바이오마커)을 많이 포함하고 있다고 알려져 있다. 인체에 부착 혹은 착용하여 이러한 생체 용액을 분석하고 바이오 마커 정보를 주고받을 수 있는 웨어러블 바이오센서 기술은 전세계 기업, 연구소, 대학에서 활발하게 개발하고 있다. 생체 내 바이오 마커와 결합하는 효소들은 바이오 마커와 전자를 직접 주고받을 수 있는 산화환원센터를 가지고 있는 경우가 많다. 기존에 널리 사용되는 효소 기반 바이오센서는 화학적 매개체를 통하여 효소의 이러한 산화환원센터로부터 전자를 전극으로 전달 받았는데 (제 2세대 바이오센서), 이러한 전자 매개체로 사용되는 물질은 대게 독성이 높은 화학 물질이어서 인체에 적용하는 웨어러블 디바이스에 적용하는데 한계가 있었다. 반면, 효소의 산화환원센터와 전극이 매개체 없이 직접적으로 전자를 주고받는 방식인 직접-전자-전달 (Direct-Electron-Transfer, DET) 방식을 이용하는 제 3세대 바이오센서의 경우, 화학적 매개체를 이용하지 않으므로 인체 안정성이 높고, 동작 전압이 낮아 방해요소인자들에 대해서 둔감하므로 선택성도 매우 높다고 알려져 있다. 그러나 DET 방식의 제 3세대 바이오센서는, 효소의 산화환원센터와 전극 간의 저항이 높아 그 전자 전달 효율이 낮은것이 큰 문제였다. 특히 눈물, 땀, 타액 등의 생체 용액 내에 있는 건강지표 인자들은 혈액 내에 존재할 때 보다 그 농도가 수십 배 이상 낮은 경우가 많아 전자 전달 효율이 낮은 DET 방식을 적용하기는 더욱 어려웠다. 나노전자소재를 전극으로 이용하면 효소와 긴밀한 전기적 접촉이 가능해 효소와 전극 간의 저항을 낮춰 직접적인 전자 전달의 효율을 높일 수가 있다. 그러나 기존의 나노 소재 기반 효소 전극 공정은 전극을 기능화 시키는 과정에서 전극의 전기적 특성이 저하되는 경우가 많아 효율이 높지 않거나 유연집적소자공정에 적합하지 않아 웨어러블 디바이스에 적용하기 어려웠다. 이현정 박사팀은 고전도성 나노전자소재인 단겹탄소나노튜브와 강한 결합력을 가진 실 모양의 바이오 물질을 이용하여 (M13 박테리오파지) 단겹탄소나노튜브를 나노그물 구조의 대면적 전도성 나노메쉬 전극으로 형성하고, 고분자 전해질 층을 이용하여 효소를 나노메쉬 전극과 결합시켜 전자전달효율이 높은 나노메쉬 효소전극을 개발하였다. 나노메쉬 전극은 기계적인 유연성이 뛰어나고 수용액에서 대면적으로 형성되므로 단순한 공정으로 유연소자제작이 가능하다. 또한 연구진이 개발한 바이오 물질은 수용액에서 음전하를 띄고 있어서 반대 전하를 띄는 고분자 전해질 층을 이용하여 효소를 나노메쉬 전극에 효율적으로 고정화시킬 수 있었다. 연구팀이 개발한 나노메쉬 효소전극을 이용한 제 3세대 글루코스센서는 그 민감도가 세계적 수준의 값을 나타내었으며, 특히 세계 최초로 구현한 제 3세대 유연글루코스센서도 비슷한 수준의 민감도를 보임으로써 차세대 헬스케어용 웨어러블 바이오센서로의 높은 적용 가능성을 보여주었다. 연구팀은 또한 개발한 나노메쉬 효소전극 기술을 적용하여 글루코스센서에 쓰이는 글루코스옥시다아제 효소를 비롯하여 콜레스테롤 옥시다아제, 락테이트 옥시다아제 등 총 8가지 다른 효소에 대해서 전자를 직접 주고받을 수 있음을 증명하였다. 또한 나노메쉬 효소 플랫폼은 바이오 플루이드 내 주요 방해 인자들로 알려진 ascorbic acid, uric acid, acetaminophen등에는 반응을 하지 않아서 바이오 센서의 가장 큰 이슈 중 하나인 선택성 측면에서도 뛰어난 특성을 나타내었다. 따라서 본 연구를 통하여 개발된 기술을 적용한 웨어러블 디바이스를 이용하면 글루코스뿐만 아니라 젖산, 콜레스테롤, 과산화수소 등 여러 건강지표 인자들을 효과적으로 모니터링 할 수 있을 것으로 기대된다. 본 연구는 KIST의 주요 연구 사업으로 수행되었으며, 연구결과는 재료 연구 분야의 학술지인 어드밴스드 머티리얼즈 (Advanced Materials)지에 12월 14일자에 온라인으로 게재되었다. * (논문명) Direct Electron Transfer of Enzymes in a Biologically Assembled Conductive Nanomesh Enzyme Platform - (제1저자) 한국과학기술연구원 이승우 박사 - (교신저자) 한국과학기술연구원 이현정 박사 <그림자료> <그림 1> 왼쪽: 효소와 직접 전자를 주고받기 위하여 나노전극으로 사용한 나노메쉬소재의 이미지와 그 나노구조의 개략도. 오른쪽: 나노메쉬기반 효소전극 플랫폼의 나노구조의 개략도. 전자를 주고받을 수 있는 효소(enzyme)가 고분자 전해질 층 (polyelectrolyte)을 통하여 나노메쉬에 접촉되어 있음. 나노메쉬에서 단겹탄소나노튜브는 전기를 통하는 나노 전극역할을 하며, M13 phage 바이오 물질(M13 phage)은 나노메쉬의 나노구조를 제어할 뿐 아니라 대면적 나노메쉬구조를 유지하고 안정화하는 역할도 하게 된다. 또한 표면에 전하를 띄고 있어서 고분자 전해질 층을 이용하여 효소를 고정화시키는 역할도 한다. <그림2> 나노메쉬기반 글루코스 옥시다아제 효소 (GOx) 전극(GOx/PEI/Nanomesh/Au)과 나노메쉬가 없는 일반적인 금 효소 전극(GOx/PEI/Au)에서 글루코스옥시다아제 효소의 직접전자전달 효율을 비교한 그림. 직접전자전달효율이 높을수록 FAD redox에서 나오는 전류피크의 크기가 크다. 나노메쉬가 형성된 전극에서 효소의 전자전달효율을 매우 높임을 알 수 있다. <그림3> 나노메쉬 효소전극을 이용한 제3세대 유연 글루코스센서. 글루코스의 양이 증가할수록 직접전자전달에 의한 전류크기가 줄어드는데, 그 줄어드는 정도가 글루코스의 양에 비례함을 이용하여 글루코스센서를 구현할 수 있다. 나노메쉬 효소 전극기반 글루코스센서는 유연할 뿐만 아니라 방해 물질에 대하여 선택성이 뛰어나고 감도가 좋아 눈물, 땀과 같은 생체 용액 내에서 낮은 농도를 지닌 표적 물질만 모니터링 할 수 있는 고성능 웨어러블 센서로 유용하게 응용될 수 있다. <그림4> 나노메쉬 효소전극 기반 바이오 센싱 플랫폼. 건강지표와 관련이 있는 콜레스테롤, 젖산, 과산화수소 등 다양한 성분과 반응하는 효소에 대하여도 전자를 직접주고 받을 수 있으며 바이오센서로 응용이 가능함.
- 75
- 작성자스핀융합연구단 이현정 박사팀
- 작성일2015.12.17
- 조회수30675
-
74
KIST, 세계최초로 알츠하이머병의 근원적 치료 가능한 신약 개발
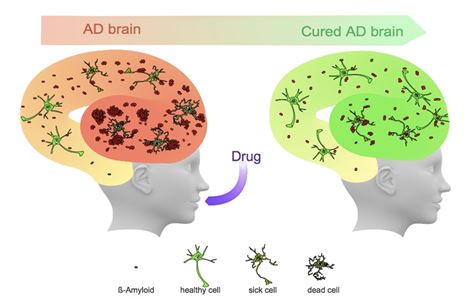
KIST, 세계최초로 알츠하이머병의 근원적 치료 가능한 신약 개발 - 알츠하이머병의 원인 독성 단백질 완벽히 제거하고, 인지 능력을 정상 수준으로 회복 - 독성 없고 흡수율 높아 물에 타먹을 수 있는 소분자 물질 고령화 시대 대표적 질환인 알츠하이머병은 치매의 60~80%를 차지할 정도로 치매 중 가장 흔한 퇴행성 뇌질환이다. 알츠하이머병은 예방 및 치료 방법이 없는 질병으로, 약 10년여에 걸쳐 진행되며 치료기간동안 오랜 약물 투약이 필요하다. 그래서 섭취하기 쉽고 부작용이 적으며 체내에 들어갔을 때 안정성이 뛰어난 의약품이 필요하다. 한국과학기술연구원(KIST, 원장 이병권) 연구진은 알츠하이머병을 근원적으로 치료할 수 있는 신약 후보물질을 개발했다. 식수에 타서 마셨을 때 알츠하이머병의 원인 단백질인 베타아밀로이드를 뇌에서 완벽하게 제거하고 치매 증상을 정상 수준으로 회복시켜줄 수 있는 물질로 세계적으로 처음 보고되는 치료방법이다. KIST 뇌과학연구소 김영수 박사, 김동진 소장 연구팀은 경구로 투약한 EPPS라는 신약후보물질이 알츠하이머병을 유발하는 베타아밀로이드 단백질의 응집체를 뇌에서 완벽히 제거하고 기억력 감퇴와 인지능력 저하 등의 치매 증상을 치료할 수 있다고 밝혔다. (주: EPPS는 화합물 3-[4-(2-Hydroxyethyl)-1-piperazinyl]propanesulfonic acid의 줄임말) 연구팀은 알츠하이머병의 원인 단백질로 알려진 베타아밀로이드 단량체는 정상인의 뇌에도 분포되어있으나 알츠하이머 환자의 뇌에서만 응집되어있다는 점에서 본 연구의 아이디어를 착안했다. 단백질의 응집체와 다양한 합성화합물들 간의 상호 반응을 조사했고, EPPS가 베타아밀로이드 응집체를 독성이 없는 단량체 형태로 풀어준다는 연구결과를 도출했다. 이 결과를 바탕으로 식수에 EPPS을 녹인 후 알츠하이머병에 걸린 생쥐에게 3개월간 투여하여 뇌기능의 변화를 관찰했고, 인지 능력을 관장하는 뇌의 해마와 대뇌피질 부위에 있는 베타아밀로이드 응집체가 모두 사라진 것을 발견했다. 생쥐의 기억력 검사로 쓰이는 Y-maze, Fear conditioning 및 Morris water maze와 같은 행동시험에서 약물을 섭취한 알츠하이머 생쥐의 인지 기능이 정상 수준으로 회복되었다. 또한, 알츠하이머병이 진행되면서 나타나는 증상인 신경 염증이 사라졌을 뿐만 아니라 뇌 기능 저하를 유발하는 GABA 급성분비 또한 억제 된다는 것을 확인했다. 주목할 만한 특징은 EPPS가 뇌의 혈관장벽을 투과하여 경구로 섭취하여도 뇌에서 흡수가 잘 되는 물질이라는 점이다. 이런 이유로 별도의 복잡한 투약절차 없이 식수 등 음식으로 EPPS를 섭취해도 효과가 높다. 이번 연구 결과를 토대로 연구팀은 EPPS가 의약품으로 허가될 수 있도록 전임상 및 임상 연구를 추진하고 있다. 또한, 이 물질은 알츠하이머병의 혈액 진단 시스템 개발 사업과 연계되어 알츠하이머병의 진단과 치료를 동시에 수행할 수 있는 연구도 진행 중이다. 본 연구 결과는 12월 9일 세계적으로 권위있는 과학지인 ‘Nature Communications’에 ‘EPPS rescues hippocampus-dependent cognitive deficits in APP/PS1 mice by disaggregation of amyloid-ß oligomers and plaques’라는 제목으로 게재되었다. (주: amyloid-ß: 아밀로이드-베타) 이 연구는 KIST 뇌과학연구소 기관고유사업의 일환으로 추진되었다. KIST 김영수 박사는 “이번에 발견한 EPPS의 알츠하이머병 치료 효능을 신약 개발에 적용하면 인체 친화적이고 부작용이 없으며 효능이 우수한 치료제를 개발할 수 있을 것으로 보인다”며, “본 연구의 결과를 토대로 알츠하이머병의 병리학적 원인 규명 및 근원적 치료제 개발 연구에 더욱 힘쓸 예정”이라고 하였고, KIST 김동진 뇌과학연구소장은 “임상 연구를 수행해봐야 알 수 있겠지만, 현재까지의 연구결과만으로도 치매의 근원적 치료제 개발의 새로운 방향을 제시했다는 점에서 그 의미가 크다”라고 말했다. <그림자료> 그림1) 신약후보물질에 의한 알츠하이머병 치료 효과 (원인물질제거), 치매 생쥐 뇌(좌), 약물 투약 후 치매 생쥐 뇌(우) 알츠하이머병이 유발된 생쥐 모델에 EPPS를 투약한 결과 병을 유발하는 베타아밀로이드 응집체가 뇌에서 거의 사라졌음. 그림2) 신약후보물질의 알츠하이머병 치료 기전 알츠하이머병의 원인 독성 단백질 완벽히 제거하고 인지 능력을 정상 수준으로 회복
- 73
- 작성자뇌과학연구소 김영수 박사, 김동진 소장 연구팀
- 작성일2015.12.08
- 조회수33826